癌症已是全球人类致死第二大死因。从全球情况来看,近六分之一的死亡由癌症造成。如何靶向的结合光动力力学治疗癌症已是众多科研工作者致力于探究的方向。其中,利用修饰过的二氧化硅纳米颗粒作为纳米反应器,以增强对肿瘤微环境的酸响应,能够进一步靶向细胞器,结合 PDT 治疗肿瘤已被证实其临床应用价值。
成果简介
近日,中国苏州大学刘庄教授和李斌教授(共同通讯作者)等人开发了一种多阶段响应的智能纳米粒子系统,通过解决传统 PDT 中的一些问题来提高 PDT 的治疗效果。将过氧化氢酶(CAT)和一种水溶性的 H2O2 分解酶封装在空心的二氧化硅纳米颗粒内部空腔里,和 Ce6(一种光敏剂)一起掺杂到二氧化硅晶格结构中,通过简单的“一锅法”反应制备。研究成果以题为“Smart nano-reactors for pH-responsive tumor homingmitochondria-targeting, andenhanced photodynamic-immunotherapy of cancer”发布在国际著名期刊 Nano Letters 上。
图文导读
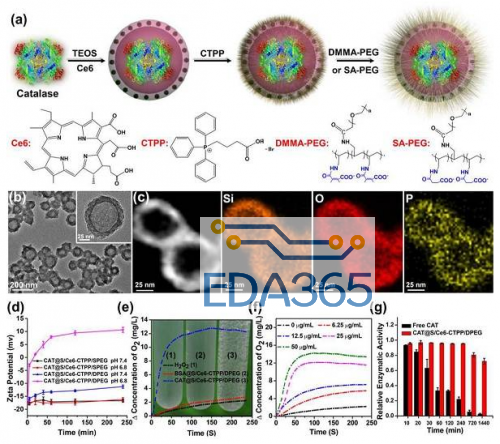
图 1. 材料的制备与表征
(a)CAT@S/Ce6-CTPP/DPEG 的制备过程;
(b)CAT@S/Ce6-CTPP/DPEG 的 TEM 图;
(c)CAT@S/Ce6-CTPP/DPEG 的 HAADF-STEM 图和元素图;
(d)CAT@S/Ce6-CTPP/SPEG 和 CAT@S/Ce6-CTPP/DPEG 在不同 pH 值时的 zeta 电位值;
(e)BSA@S/Ce6-CTPP/DPEG 和 CAT@S/Ce6-CTPP/DPEG 生成氧气量的变化图;
(f)不同浓度的 CAT@S/Ce6-CTPP/DPEG 的生成氧气量的变化图;
(g)孵育蛋白酶 K 后,游离过氧化氢酶和 CAT@S/Ce6-CTPP/DPEG 的酶活性变化图。

图 2.PDT 的体外实验
(a)CAT@S/Ce6-CTPP/DPEG 增强 PDT 作用的过程原理图;
(b)不同浓度的 CAT@S/Ce6-CTPP/DPEG 对 4T1 的毒性实验;
(c)不同浓度 Ce6 的 BSA@S/Ce6-CTPP/DPEG 和 CAT@S/Ce6-CTPP/DPEG 对 4T1 的毒性实验;
(d)CAT@S/Ce6-CTPP/SPEG 和 CAT@S/Ce6-CTPP/DPEG 在不同 PH 值的共聚焦图像;
(e)不同浓度 Ce6 的 CAT@S/Ce6-CTPP/SPEG 和 CAT@S/Ce6-CTPP/DPEG 在不同 PH 值下对 4T1 的毒性实验;
(f)CAT@S/Ce6/DPEG 和 CAT@S/Ce6-CTPP/DPEG 在不同时间点细胞里的位置的共聚焦图像;
(g)根据(f)中的皮尔逊相关系数(Rr)统计值;
(h)不同浓度 Ce6 的 CAT@S/Ce6/DPEG 和 CAT@S/Ce6-CTPP/DPEG 对 4T1 的毒性实验。

图 3. 体内成像和肿瘤氧化调制实验
(a)CAT@S/Ce6-CTPP/SPEG 和 CAT@S/Ce6-CTPP/DPEG 的小鼠体内荧光成像图;
(b)正常器官和肿瘤处的体外荧光成像图;
(c)主要器官和肿瘤的体外荧光成像的量化图;
(d)小鼠肿瘤切片的共聚焦图像;
(e)小鼠 4T1 肿瘤的肿瘤氧合状态的 PA 图像;
(f)基于(e)PA 成像的肿瘤血氧饱和度的量化图;
(g)不同治疗组的肿瘤切片免疫荧光染色显微图。

图 4.CAT@S/Ce6-CTPP/DPEG 进行 PDT 活体治疗实验
(a)4T1 模型下,PDT 治疗后的肿瘤生长曲线图;
(b)治疗结束后,不同组的平均肿瘤重量图;
(c)在研究结束后,从不同组小鼠体内取出的所有肿瘤照片图;
(d)不同时间下,不同组的小鼠体重变化图;
(e)H&E 和 TUNEL 染色的肿瘤切片图。

图 5. 结合 PDT 与 CAT@S/Ce6-CTPP/DPEG 检查点阻塞免疫治疗
(a)梳理 PDT 与抗 -PD-L1 治疗实验设计图;
(b)左边肿瘤生长曲线图;
(c)左边第 18 天时,平均肿瘤重量图;
(d)左边第 18 天时,CTL 渗透百分比图;
(e)右边肿瘤生长曲线图;
(f)右边第 18 天时,平均肿瘤重量图;
(g)右边第 18 天时,CTL 渗透百分比图;
(h)不同治疗 7 天后,从小鼠血清中检测 IFN-γ水平;
(i)治疗期间,小鼠体重变化图;
(j)PDT 与抗 -PD-L1 联合治疗的机理说明图。
小结
研究开发了具有 pH 响应能力的电荷转换、线粒体靶向和包封过氧化氢酶的中空二氧化硅纳米颗粒,并将 Ce6 掺杂作为一种用于改进癌症 PDT 治疗的智能纳米反应器。使得肿瘤微酸环境处电荷由负变正,有利于细胞内化和肿瘤处滞留,增强对线粒体的靶向和 PDT 对肿瘤细胞的杀伤力,同时产生 ROS。为制备抗肿瘤纳米材料提供一些新的策略与方法。


 APP下载
APP下载 登录
登录














 热门文章
热门文章